Оплата и способы получения
Инструкция на Пролиа 60 мг/мл, раствор для подкожного введения, 1 мл, 1 шт.
Состав
| Раствор для подкожного введения | 1 мл |
| каждый предварительно заполненный шприц содержит | |
| активное вещество: | |
| деносумаб | 60 мг |
| вспомогательные вещества: сорбитол (Е420) — 47 мг; уксусная кислота ледяная — 1 мг; полисорбат 20 — 0,1 мг; натрия гидроксид — до рН 5,0–5,5; вода для инъекций — до 1 мл |
Описание
Прозрачная жидкость, от бесцветного до светло-желтого цвета, практически свободная от видимых включений.
Фармакодинамика
Механизм действия
Деносумаб представляет собой полностью человеческое моноклональное антитело (IgG2), обладающее высокой аффинностью и специфичностью к лиганду рецептора активатора ядерного фактора κВ (RANKL), и тем самым препятствует активации единственного рецептора RANKL — активатора ядерного фактора κВ (RANK), расположенного на поверхности остеокластов и их предшественников. Таким образом, предотвращение взаимодействия RANKL/RANK ингибирует образование, активацию и продолжительность существования остеокластов. В результате деносумаб уменьшает костную резорбцию и увеличивает массу и прочность кортикального и трабекулярного слоев кости.
Фармакодинамические эффекты
Назначение деносумаба в дозе 60 мг приводило к быстрому уменьшению сывороточных концентраций маркера резорбции костной ткани — 1С-телопептида (СТХ) — приблизительно на 70% в течение 6 ч после подкожного введения и приблизительно на 85% в течение последующих 3 дней. Уменьшение концентрации СТХ оставалось стабильным в 6-месячном интервале между дозированием. Скорость снижения концентрации СТХ в сыворотке крови частично уменьшалась при снижении концентрации деносумаба в сыворотке крови, что отражает обратимость влияния деносумаба на ремоделирование кости. Данные эффекты наблюдались на протяжении всего курса лечения. Соответственно физиологической взаимосвязи процессов образования и резорбции при ремоделировании костной ткани, наблюдалось уменьшение содержания маркеров образования кости (например костноспецифической ЩФ и сывороточного N-концевого пропептида коллагена I типа) с первого месяца после введения первой дозы деносумаба. Маркеры ремоделирования кости (маркеры образования кости и резорбции кости), как правило, достигали концентраций периода до начала лечения не позднее чем через 9 мес после приема последней дозы препарата. После возобновления лечения деносумабом степень снижения концентраций СТХ была сходна со степенью снижения концентрации СТХ в начале курса лечения деносумабом.
Было показано, что перевод с лечения алендроновой кислотой (средняя продолжительность применения — 3 года) на деносумаб приводит к дополнительному снижению концентрации СТХ в сыворотке по сравнению с группой женщин в постменопаузе с низкой костной массой, продолжавших лечение алендроновой кислотой. В то же время изменения содержания кальция в сыворотке были одинаковыми в обеих группах.
В экспериментальных исследованиях ингибирование RANK/RANKL одновременно со связыванием остеопротегерина с Fc-фрагментом (OPG-Fc) приводило к замедлению роста кости и нарушению прорезывания зубов. Поэтому лечение деносумабом может тормозить рост костей с открытыми зонами роста у детей и приводить к нарушениям прорезывания зубов.
Иммуногенность
Деносумаб — человеческое моноклональное антитело, поэтому, как и для других ЛС белковой природы, существует теоретический риск иммуногенности. Более чем 13000 пациентов были обследованы на предмет образования связывающих антител с использованием метода чувствительной электрохемилюминесценции в сочетании с иммунологическим анализом. Менее чем у 1% пациентов, принимавших деносумаб в течение 5 лет, определялись антитела (включая существовавшие ранее, транзиторные и растущие). Серопозитивные пациенты были далее обследованы на предмет образования нейтрализующих антител, используя хемилюминисцентный анализ в культуре клеток in vitro, нейтрализующих антител не обнаружено. Не было выявлено изменений фармакокинетического профиля, токсического профиля или клинического ответа, обусловленных образованием антител.
Клиническая эффективность
Лечение остеопороза в постменопаузе
У женщин с постменопаузальным остеопорозом Пролиа™ увеличивает минеральную плотность кости, уменьшает частоту переломов шейки бедра, вертебральных и невертебральных переломов. Эффективность и безопасность деносумаба в лечении постменопаузального остеопороза была доказана в исследовании длительностью 3 года. Результаты исследования показывают, что деносумаб существенно, в сравнении с плацебо, снижает риск возникновения вертебральных и невертебральных переломов, переломов шейки бедра у женщин с остеопорозом в постменопаузе. В исследование было включено 7808 женщин, из которых у 23,6% отмечались часто встречающиеся переломы позвонков. Все три конечные точки эффективности в отношении переломов достигали статистически значимых значений, оцениваемых по предварительно заданной последовательной схеме тестирования.
Снижение риска возникновения новых вертебральных переломов при применении деносумаба в течение более чем 3 лет оставалось стабильным и значимым. Риск снижался независимо от 10-летней вероятности возникновения крупных остеопоротических переломов. На снижение риска также не влияли наличие часто встречающихся переломов позвонков в анамнезе, невертебральные переломы, возраст пациентов, минеральная плотность кости, уровень ремоделирования кости и предшествующая терапия по поводу остеопороза.
У женщин старше 75 лет в постменопаузе деносумаб уменьшал частоту возникновения новых вертебральных переломов, и, по данным post hoc анализа, уменьшал частоту переломов шейки бедра.
Уменьшение частоты возникновения невертебральных переломов наблюдалось независимо от 10-летней вероятности возникновения крупных остеопоротических переломов. Деносумаб существенно, по сравнению с плацебо, увеличивал минеральную плотность кости во всех анатомических областях. Минеральную плотность кости определяли через 1, 2 и 3 года после начала терапии. Сходное влияние на минеральную плотность кости отмечено в поясничном отделе позвоночника независимо от возраста, расовой принадлежности, индекса массы тела (ИМТ), минеральной плотности кости и ремоделирования кости. Гистологические исследования подтвердили нормальную архитектонику кости и, как и ожидалось, снижение костного ремоделирования по сравнению с плацебо. Не отмечено патологических изменений, включая фиброз, остеомаляцию и нарушение архитектоники костной ткани.
Клиническая эффективность при лечении потери костной массы, вызванной гормондепривационной терапией или терапией ингибиторами ароматазы
Лечение потери костной массы, вызванной депривацией андрогенов
Эффективность и безопасность деносумаба при лечении потери костной массы, ассоциированной со снижением концентрации андрогенов, были доказаны в 3-летнем исследовании, включавшем 1468 пациентов с неметастатическим раком предстательной железы. Существенное увеличение минеральной плотности кости определяли в поясничном отделе позвоночника, всей бедренной кости, шейке бедренной кости, вертеле бедренной кости спустя 1 мес после приема первой дозы. Увеличение минеральной плотности кости в поясничном отделе позвоночника не зависело от возраста, расовой принадлежности, географического региона, ИМТ, начальных значений минеральной плотности кости, ремоделирования кости; продолжительности проведения гормондепривационной терапии и наличия вертебрального перелома в анамнезе.
Деносумаб значительно уменьшал риск возникновения новых вертебральных переломов на протяжении 3 лет применения. Уменьшение риска наблюдалось через 1 год и через 2 года после начала терапии. Деносумаб также снижал риск возникновения более чем одного остеопоротического перелома любой локализации.
Лечение потери костной массы у женщин, получающих терапию ингибиторами ароматазы по поводу рака молочной железы
Эффективность и безопасность деносумаба в лечении потери костной массы, вызванной адъювантной терапией ингибитором ароматазы, оценивалась в 2-летнем исследовании, включавшем 252 пациентки с неметастатическим раком молочной железы. Деносумаб значительно увеличивал минеральную плотность кости во всех анатомических областях, по сравнению с плацебо, в течение 2 лет. Увеличение минеральной плотности кости наблюдалось в поясничном отделе позвоночника спустя месяц после приема первой дозы. Положительное влияние на минеральную плотность кости в люмбальном отделе позвоночника отмечали вне зависимости от возраста, продолжительности терапии ингибитором ароматазы, ИМТ, предшествующей химиотерапии, предшествующего использования селективного модулятора рецепторов эстрогена (СМРЭ) и времени, прошедшего от начала менопаузы.
Фармакокинетика
При п/к введении деносумаб характеризуется нелинейной фармакокинетикой, дозозависимой в широком диапазоне доз, и дозозависимым увеличением экспозиции для дозы в 60 мг (или 1 мг/кг) и выше.
Всасывание
После п/к введения деносумаба в дозе 60 мг биодоступность составила 61% и Cmax — 6 мкг/мл (диапазон 1–17 мкг/мл), данные параметры наблюдались через 10 дней (диапазон 2–28 дней). После достижения Cmax содержание препарата в сыворотке крови снижалось с T1/2 26 дней (диапазон 6–52 дня) и далее в течение 3 мес (диапазон 1,5–4,5 мес). У 53% пациентов деносумаб не обнаруживался в сыворотке крови после 6 мес от последнего введения препарата.
Распределение
Не наблюдалось изменений фармакокинетических параметров деносумаба, а также кумуляции за все время приема многократных доз препарата по 60 мг каждые 6 мес.
Метаболизм
Деносумаб состоит из аминокислот и углеводов, как обычный иммуноглобулин. На основании данных доклинических исследований, ожидается, что метаболизм деносумаба будет происходить по пути клиренса иммуноглобулинов, результатом которого будет распад на небольшие пептидные цепи и отдельные аминокислоты.
Выведение
На основании доклинических данных, выведение деносумаба будет происходить по пути выведения всех иммуноглобулинов, результатом которого будет распад на небольшие пептидные цепи и отдельные аминокислоты.
Отдельные группы пациентов
Пациенты пожилого возраста (65 лет или старше). Возраст не оказывает значимого влияния на фармакокинетику деносумаба, по данным фармакокинетического анализа в популяции пациентов от 28 до 87 лет.
Дети и подростки (до 18 лет). Фармакокинетика у детей не изучалась.
Расовая принадлежность. Фармакокинетика деносумаба не зависит от расовой принадлежности.
Пациенты с почечной недостаточностью. В исследовании данных 55 пациентов с различной степенью почечной недостаточности, включая пациентов, находящихся на диализе, степень почечной недостаточности не оказывала влияния на фармакокинетику и фармакодинамику деносумаба, поэтому не требуется коррекция режима дозирования деносумаба при хронической почечной недостаточности.
Хроническая печеночная недостаточность. Исследований влияния недостаточности функции печени на фармакокинетику деносумаба не проводилось.
Пролиа: Показания
лечение постменопаузального остеопороза;
лечение потери костной массы у женщин, получающих терапию ингибиторами ароматазы по поводу рака молочной железы и у мужчин, с раком предстательной железы, получающих гормондепривационную терапию.
Способ применения и дозы
Введение
Проведение инъекции препарата требует предварительного обучения — см. рекомендации по введению препарата, приведенные в конце настоящего раздела.
Доза
Рекомендуемая доза препарата Пролиа™ — одна п/к инъекция 60 мг каждые 6 мес. В течение курса лечения рекомендуется дополнительно принимать препараты кальция и витамин D.
Применение у отдельных групп пациентов
Дети. Препарат Пролиа™ не рекомендован к применению в педиатрии, т.к эффективность и безопасность данного препарата не изучались в этой возрастной группе.
Пациенты пожилого возраста. Основываясь на имеющихся данных об эффективности и безопасности препарата в данной возрастной группе, не требуется коррекция режима дозирования препарата (см. «Фармакокинетика», Отдельные группы пациентов).
Почечная недостаточность
Основываясь на имеющихся данных об эффективности и безопасности препарата в данной группе пациентов, не требуется коррекция режима дозирования препарата (см. «Фармакокинетика», Отдельные группы пациентов).
У пациентов с тяжелой почечной недостаточностью (Cl креатинина <30 мл/мин) или находящихся на диализе существует большой риск развития гипокальциемии. Таким пациентам необходимо дополнительно принимать препараты кальция и витамин D.
Печеночная недостаточность. Эффективность и безопасность не изучались.
Инструкция по использованию
Следует оценить раствор перед введением на предмет наличия включений или изменения цвета. Раствор нельзя использовать при помутнении или изменении цвета. Не встряхивать.
Чтобы избежать дискомфорта в месте введения, следует согреть раствор до комнатной температуры (до 25 °C) перед инъекцией, а затем медленно ввести все содержимое предварительно заполненного шприца. Шприц с остатками препарата выбросить. Подробные рекомендации по самостоятельному п/к введению препарата включены в данную инструкцию по медицинскому применению.
Любые количества неиспользованного препарата или неиспользованные материалы должны быть уничтожены в соответствии с местными требованиями.
Инструкции по введению препарата Пролиа™, предварительно заполненные шприцы с защитным устройством для иглы
В этом разделе приводится информация по правильному проведению инъекции предварительно заполненным шприцем (ПЗШ) с защитным устройством для иглы. Очень важно, чтобы перед тем, как вы приступите к самостоятельным инъекциям, лечащий врач, медицинская сестра подробно проинструктировали вас по технике выполнения инъекции. Если у вас возникнут вопросы по технике выполнения инъекции, то обратитесь к лечащему врачу или медицинской сестре.

Перед началом инъекции
Внимательно прочитайте все инструкции перед использованием ПЗШ.
Для уменьшения риска случайного укола каждый ПЗШ оснащен предохранителем — защитным устройством для иглы, которое автоматически активируется для закрывания иглы после завершения инъекции.
Не пытайтесь разбирать ПЗШ или активировать предохранитель перед инъекцией. Не используйте ПЗШ, если колпачок был удален или предохранитель иглы был активирован.
Как использовать предварительно заполненный шприц?
Ваш врач назначил вам препарат Пролиа™ ПЗШ для подкожных инъекций. Вы должны ввести все содержимое шприца однократно и повторить инъекцию через 6 мес, как назначено лечащим врачом.
Оборудование
Для самостоятельной инъекции вам потребуется:
1. Новый ПЗШ препарата Пролиа™;
2. Смоченные спиртом тампоны или сходные материалы.
Что вы должны сделать до самостоятельного введения Пролиа™ подкожно?
1. Достать шприц из холодильника. Не брать ПЗШ за поршень или защитный колпачок, это может повредить устройство.
2. Оставить ПЗШ при комнатной температуре для более комфортной инъекции. Не подогревать ПЗШ каким-либо другим способом (например в микроволновой печи либо в горячей воде). Не оставлять шприц под прямыми солнечными лучами.
3. Не встряхивать ПЗШ.
4. Не удалять колпачок ПЗШ до тех пор, пока вы не готовы к инъекции.
5. Проверить срок годности ПЗШ. Срок годности указан на упаковке как «ГОДЕН ДО: ММ.ГГГГ». Не использовать ПЗШ после последнего дня указанного месяца хранения.
6. Проверить внешний вид препарата Пролиа™. Раствор должен быть прозрачным, бесцветным или светло-желтым. Если раствор помутнел или окрашен иначе, препарат использовать нельзя.
7. Выбрать комфортное, хорошо освещенное место и чистую поверхность, где можно удобно расположить все необходимые материалы.
8. Тщательно вымыть руки.
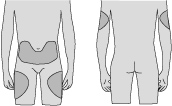
Как правильно выбрать место для инъекции?
Лучше всего делать инъекции в верхнюю часть бедер и живота. Если инъекции вам делает кто-то другой, можно использовать тыльную поверхность рук.
Если область, куда вы собрались делать инъекцию, покраснела или отекла, следует выбрать другое место инъекции.
Как производить инъекцию?
1. Продезинфицировать место инъекции с помощью смоченного в спирте тампона.
2. Во избежание изгиба иглы, аккуратно потянуть колпачок с иглы сразу без скручивания, как показано на рисунке. Не дотрагиваться до иглы и не нажимать на поршень.
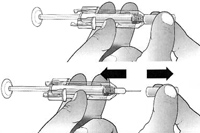
3. Если внутри ПЗШ видны маленькие пузырьки воздуха, нет необходимости удалять их перед инъекцией. Введение раствора с пузырьками воздуха является безопасным.
4. Зажать кожу (не сдавливая) между большим и указательным пальцами. Ввести иглу, как показывал вам доктор или медицинская сестра.
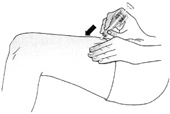
5. Медленно и плавно надавить на поршень, одновременно придерживая кожную складку. Надавливать на поршень следует до тех пор, пока шприц не опустеет. Предохранитель иглы не сработает, пока шприц не опустеет.
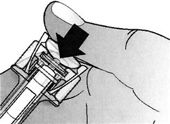
6. Пока поршень нажат, удалите иглу из кожи и отпустите кожную складку.
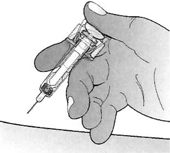
Затем отпустите поршень и позвольте шприцу подняться вверх до тех пор, пока вся игла не покроется предохранителем иглы.
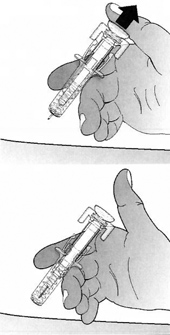
7. Если предохранитель не активировался, возможно, что вы не выполнили инъекцию полностью. Позвоните лечащему врачу, если считаете, что вы не получили полную дозу.
Не надевать колпачок на иглу.
8. Если выступит кровь в месте инъекционного прокола, аккуратно стереть ее ватным тампоном или тканью. Не растирать место инъекции. При необходимости, можно заклеить место инъекции пластырем.
9. Использовать один ПЗШ только для одной инъекции. Не использовать оставшийся в шприце препарат.
Помните: при возникновении проблем обратитесь за помощью или советом к лечащему врачу или медицинской сестре.
Уничтожение использованных шприцов
Не надевать обратно колпачок на использованный шприц.
Хранить использованный шприц в недоступном для детей месте.
Использованный шприц должен быть утилизирован в соответствии с местными правилами. Спросите у врача или провизора, как уничтожить препарат, если он больше не требуется. Эти меры помогут защите окружающей среды.
Применение при беременности и кормлении грудью
Нет каких-либо данных по применению препарата во время беременности. Пролиа™ не рекомендуется для применения у беременных женщин.
В токсикологических исследованиях на низших приматах было показано, что в дозах, 100-кратно превышающих рекомендуемые для клинического применения, деносумаб не оказывал влияния на фертильность или развитие плода.
Эксперименты на мышах с выключенным геном показали, что отсутствие RANKL может приводить к нарушению развития лимфатических узлов у плода, а в постнатальном периоде может быть причиной нарушения прорезывания зубов и роста костей; также возможно влияние на созревание молочной железы, что может приводить к ослаблению лактации.
Пациенткам, у которых беременность наступила во время лечения препаратом Пролиа™, следует зарегистрироваться в Программе наблюдения беременности компании Амджен. Пациенты или врачи, у которых они находятся под наблюдением, могут позвонить по телефону, указанному в конце настоящей инструкции для регистрации в Программе наблюдения.
Неизвестно, выводится ли деносумаб в грудное молоко. Поскольку известно, что потенциально деносумаб может вызывать нежелательные реакции у детей грудного возраста, необходимо или прекратить грудное вскармливание, или отменить препарат.
Пролиа: Противопоказания
повышенная чувствительность к любому из компонентов препарата;
гипокальциемия.
Пролиа: Побочные действия
Данные, полученные при контролируемом применении в клинических исследованиях.
Нежелательные реакции приводятся по классам систем органов в терминах Медицинского словаря регуляторной деятельности (MedDRA). Частота возникновения определена следующим образом: очень часто — >1 из 10; часто — >1 из 100 и <1 из 10; нечасто — >1 из 1000 и <1 из 100; редко — >1 из 10000 и <1 из 1000; очень редко <1 из 10000.
В каждой группе систем органов и частоты сообщений нежелательные реакции приводятся по убыванию степени серьезности.
| Класс системы органов | Частота | Нежелательная реакция |
| Инфекции и инвазии | Нечасто | Воспаление подкожной клетчатки |
| Со стороны метаболизма и электролитного обмена | Очень редко | Гипокальциемия1 |
| Со стороны органов зрения | Часто | Катаракта2 |
| Со стороны кожи и подкожно-жировой клетчатки | Нечасто | Экзема3 |
| Со стороны костно- мышечной системы и соединительной ткани | Часто | Боль в конечностях |
| Редко | Остеонекроз челюсти |
1 Cм. раздел «Особые указания».
2 У мужчин, получающих андрогендепривационную терапию по поводу рака предстательной железы.
3 Включая дерматиты, аллергические дерматиты, атопический дерматит, контактный дерматит.
Передозировка
В клинических исследованиях не отмечено случаев передозировки препарата.
В клинических исследованиях вводили дозы деносумаба до 180 мг каждые 4 нед (кумулятивная доза до 1080 мг в 6 мес).
Особые указания
Рекомендуется прием препаратов кальция и витамина D во время применения препарата Пролиа™.
Гипокальциемия может быть скорректирована приемом препаратов кальция и витамина D в адекватных дозах перед началом терапии деносумабом. Рекомендуется контроль концентрации кальция у пациентов, предрасположенных к гипокальциемии (см. «Побочные действия»).
У пациентов, получающих препарат Пролиа™, могут развиться инфекции кожи и ее придатков (преимущественно воспаление подкожной клетчатки), в отдельных случаях требующие госпитализации. О таких реакциях чаще сообщалось для группы деносумаба (0,4%), чем группы плацебо (0,1%) (см. «Побочные действия»). При этом общая частота возникновения кожных инфекций сравнима в группах деносумаба и плацебо. Пациентов следует проинструктировать о необходимости незамедлительно обратиться за врачебной помощью в случае развития симптомов и признаков воспаления подкожной клетчатки.
У пациентов с распространенным раком, получавших 120 мг деносумаба каждые 4 нед, сообщалось о развитии случаев остеонекроза челюсти. Имеются отдельные сообщения о развитии остеонекроза челюсти при дозе 60 мг каждые 6 мес (см. «Побочные действия»).
Лица с аллергией на латекс не должны касаться резинового колпачка иглы (производное латекса).
Влияние на способность к вождению автотранспорта и обращению с техникой. Исследований влияния на способность к вождению автотранспортных средств и управлению механизмами не проводилось.
Форма выпуска
Раствор для подкожного введения, 60 мг/мл. В одноразовом предварительно заполненном шприце (ПЗШ) 1 мл из стекла I гидролитического класса с иглой 27G из нержавеющей стали, эластомерным колпачком и эластомерным плунжером, ламинированным фторполимером (с защитным устройством для иглы или без него). Маркированный шприц помещают в пачку картонную.
ПЗШ может быть дополнительно помещен в контурную ячейковую упаковку с термоэтикеткой. Каждую контурную ячейковую упаковку помещают в пачку картонную.
Пачка картонная снабжена отрывной карточкой-напоминанием с двумя напоминающими наклейками.
Пролиа™ представляет собой стерильный продукт и не содержит консервантов.
Условия отпуска
По рецепту.
Производитель
Амджен Европа Б.В., Минервум, 7061, NL-4817ZK, Бреда, Нидерланды.
Представитель в России ООО «Амджен».
123317, Москва, Пресненская набережная, 8, блок 1, 7-й этаж.
Тел: (495) 745-04-78; факс: (499) 995-19-65.
Характеристики
Сертификаты Пролиа 60 мг/мл, раствор для подкожного введения, 1 мл, 1 шт.


Цены в аптеках на Пролиа 60 мг/мл, раствор для подкожного введения, 1 мл, 1 шт.



История стоимости Пролиа 60 мг/мл, раствор для подкожного введения, 1 мл, 1 шт.
Цены Пролиа и наличие в аптеках в Улан-Удэ
Отзывы о Пролиа
Дистанционная торговля лекарственными препаратами осуществляется исключительно аптечными организациями, имеющими действующую лицензию на фармацевтическую деятельность, а также разрешение на дистанционную торговлю лекарственными препаратами. Дистанционная торговля рецептурными лекарственными препаратами, наркотическими и психотропными, а также спиртосодержащими лекарственными препаратами запрещена действующим законодательством РФ и не осуществляется.
На информационном ресурсе применяются рекомендательные технологии .